Factores que afectan a la velocidad de reacción Química 2 bachillerato universidad teoría explicación y ejercicios clásicos de examen , en los vídeos te enseñaré algunos TRUCOS , incidiremos en las CLAVES y entenderás todo perfectamente para sacar la máxima puntuación de este tema en el examen . También resolveremos ejercicios clásicos de exámenes
Factores que afectan a la velocidad de las reacciones químicas
VER EXPLICACIÓN DE FACTORES QUE AFECTAN A LA VELOCIDAD DE REACCIÓN
1 Naturaleza Estado de agregación y grado de división de los reactivos
Naturaleza de los reactivos: Unas sustancias reaccionan más rápido que otras simplemente por sus propiedades químicas. Por ejemplo las sustancias iónicas reaccionan más rápido por norma general que las sustancias covalentes ya que estos últimos sus enlaces son más fuertes y su ruptura requiere más energía.
Estado de agregación de los reactivos: La movilidad de las partículas en estado gaseoso es mayor que en estado líquido y estas que en estado sólido , por la teoría de colisiones , cuanto mayor movilidad mayor número de choques eficaces , mayor velocidad de reacción.
En general vgas>vlíquido>vsólido
Grado de división de los reactivos:
En el caso de los sólidos al aumentar su grado de división aumenta la superficie de contacto , por lo tanto aumentará la velocidad de la reacción
Ej. Se oxida más rápido las limaduras del hierro que una barra de hierro.
2 Concentración de los reactivos
La ecuación de velocidad en una reacción de tipo A+B →
Viene dada por v=k[A]α[B]β , la ecuación nos muestra que la velocidad de la reacción depende de la concentración de los reactivos , según avanza la reacción disminuirá la concentración de los reactivos , disminuyendo la velocidad.
Por otro lado , según la teoría de colisiones al aumentar la concentración de los reactivos aumentará el número de choque eficaces , aumentando la velocidad de la reacción.
Efecto de la presión y el volumen en gases . En los gases si aumentamos la presión , aumenta la concentración , aumentando la velocidad de la reacción y si aumentamos el volumen disminuye la concentración disminuyendo la velocidad de la reacción
Si los videos te han servido , dale al LIKE y SUSCRIBETE 🚂 http://goo.gl/CMFnu0 y activa la campanilla🔥, en época de exámenes subimos muchos ejercicios clásicos de exámenes y así estarás informado ➡ compártelo por las redes sociales y grupos de clase 😉
3 Temperatura
¿Por qué guaramos los alimentos en la nevera?
Porque así ralentizamos las reacciones químicas que hacen que se estropeen
Si aumentamos la temperatura aumentamos la velocidad de la reacción
Tenemos dos formas de explicarlo.
Por la ecuación de Arrhenius
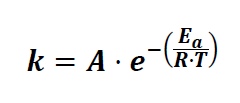
vemos que al aumentar la Temperatura aumenta la constante de la velocidad , aumentando la velocidad de la reacción.
Por la teoría de colisiones
Al aumentar la temperatura aumentará la energía cinética de las partículas , aumentando su velocidad , por lo que aumentará el número de choques eficaces , aumentado la velocidad de la reacción
4 Presencia de catalizadores
Un catalizador es una sustancia que aumenta la velocidad de la reacción sin ser consumida durante el proceso
Los catalizadores aumentan la velocidad de la reacción disminuyendo la energía de activación
Podemos verlo de dos formas :
Por los Diagramas de entalpía:
poner foto
Existen otras sustancias denominadas catalizadores negativos o inhibidores , que disminuyen la velocidad de la reacción.
Por la ecuación de Arrhenius:
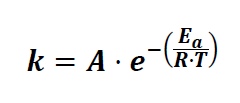
vemos que al disminuir la energía de activación aumenta la constante de la velocidad , aumentando la velocidad de la reacción.
Ejercicios resueltos Factores velocidad de reacción
Ejercicio resuelto clásico de examen Selectividad EVAU 2022
La reacción en fase gaseosa A + B → C + D es exotérmica y su ecuación cinética es v = k[A]2 . Justifique si las siguientes afirmaciones son verdaderas o falsas:
a) (0,5 puntos) El reactivo A se consume más deprisa que el B.
b) (0,5 puntos) Un aumento de la presión total produce un aumento en la velocidad de la reacción.
c) (0,5 puntos) Una vez iniciada la reacción, la velocidad es constante si la temperatura no varía.
d) (0,5 puntos) Un aumento de la temperatura disminuye la velocidad de reacción.
Índice del tema
IR AL INDICE DEL TEMA DE CINÉTICA QUÍMICA
OTRAS ENTRADAS QUE TE PUEDEN INTERESAR
CURSO DE FÍSICA Y QUÍMICA 2 ESO
CURSO DE FÍSICA Y QUÍMICA 3º ESO
CURSO DE FÍSICA Y QUÍMICA 4º ESO
CURSO DE MATEMÁTICAS 1º BACHILLERATO
CURSO DE MATEMÁTICAS SOCIALES 1º BACHILLERATO
CURSO DE FÍSICA Y QUÍMICA 1º BACHILLERATO
CURSO MATEMÁTICAS 2 BACHILLERATO
UNIVERSIDAD MATEMÁTICAS FÍSICA Y QUÍMICA








