Fórmulas para resolver ejercicios y problemas de disoluciones (soluciones )
Molaridad
Densidad
Riqueza , pureza , % masa , % peso
molalidad
Fracción molar soluto

Fracción molar disolvente
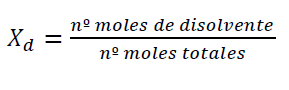
Moles

gramos por litro

NOVEDAD hemos creado una nueva entrada para que aprendáis todo sobre
PROBLEMAS Y EJERCICIOS DE DISOLUCIONES RESUELTOS EN VÍDEO
Problema 1 Disolvemos 45 gramos de amoniaco NH3 en 500 gramos de agua . Calcula el porcentaje en masa de la disolución. Ver solución
Problema 2 Calcular los gramos de una sustancia que hay que pesar para preparar una disolución de 100 ml y composición 20g/L ver solución
Ejercicios resueltos Queremos preparar 250 cm3 de disolución de sal en agua, con una concentración de 5 g/l. ¿Qué cantidad de sal debemos disolver en agua? ver solución
Ejercicios resueltos La leche tiene una densidad de 1,03 g/cm3 y 2,9 g de proteínas en 100 mL Expresa la concentración de proteínas en g/L y en tanto por ciento en masa. ver solución
Ejercicios resueltos Si en 200 mL de cierta disolución acuosa hay 12,0 g de azúcar y la densidad de dicha disolución es de 1,2 g/ml, ¿cuál es la concentración de ésta en g/L y en tanto por ciento en masa ? ver solución
Ejercicios resueltos Una disolución acuosa de hidróxido de potasio tiene una riqueza del 30% en masa . Sabiendo que la densidad de la disolución es de 1,3 g/ml calcula la masa de soluto que hay en 100 ml de disolución Ver solución
Ejercicio de examen 4 eso Marta SI
Se disuelven 180 g de sal en 800 g de agua. La densidad de la disolución es de 1,340 g/cm3 . Calcula la concentración de la disolución en: a) Tanto por ciento en masa b) Gramos por litro. Ver solución
Problema 3 Averigua la molaridad de una disolución que contiene 58,8 gramos de yoduro de calcio CaI2 , por litro. ver solución
Datos : Masas atómicas I=127 ;Ca =40
Problema 4 determina cuántos gramos de hidróxido de calcio , Ca(OH)2, hay en 500 ml de disolución 0,6 M. ver solución
Datos : Masas atómicas H=1 ; O=16 ;Ca =40
Problema 5 Calcula la molaridad de una disolución de cloruro de sodio NaCl , cuya composición es 30 g/L ver solución
Datos : Masas atómicas Cl=35,5 ;Na =23
En este enlace puedes conseguir el pdf del curso https://goo.gl/A2XdHm
Problema 6 Se prepara una disolución de cloruro de potasio , KCl , con 3g de KCl y 25 cm3 de agua . la solución resultante tiene una densidad de 1,05 g/cm3 . Calcula :
a)Molaridad solución parte 1
b)Porcentaje en masa solución parte 2
c)Composición en gramos por litro
Datos : Masas atómicas Cl=35,5 ;K =39
Ejercicio resuelto de examen enviado por un seguidor
Tenemos 350 g de una disolución de alcohol en agua al 40% en masa , calcula la masa de agua necesaria para diluir la concentración al 15% en masa
Problema 7 Calcula la molaridad de un ácido sulfúrico comercial del 95% en masa y densidad de 1,83 g/cm3
Datos : Masas atómicas H=1 ; O=16 ;S =32 ver solución
Problema 8 La etiqueta de una botella de ácido nítrico , HNO3 , indica 15,5 M y densidad 1,41 g/cm3 . Calcular su porcentaje en masa
Datos : Masas atómicas H=1 ; O=16 ;N =14 ver solución
EXPERIMENTO Adivina el color de la infusión Experimentos con ph
Explicación Dentro de la taza tenemos papel tornasol ( lo he cortado en trozos pequeños para preparar la disolución indicadora) que es un indicador de ph , En una disolución básica ( ph >7 ) , toma colores de verde oscuro a morado , en una disolución neutra ( ph=7) toma el color verde claro y en una disolución ácida ( ph < 7 ) toma colores de amarillo a rojo ver experimento
¿ que os parecen los experimentos ?
Problema 9 Calcula la molaridad de una disolución que se obtiene disolviendo 25 g de KCl en 225 g de agua, sabiendo que la densidad de la disolución es de 2,1 g/mL. Datos: A(K)=39; A(Cl)=35,5
Sol: 2,86 M ver solución
Problema 10¿Cuántos gramos de HNO3 se encuentran en 200 mL de una disolución 2,5 M? Datos: A(H)=1;A(N)=14; A(O)=16;
Sol: 31,5 gramos ver solución
Problema 11El HCl comercial contiene un 35% en masa de ácido y su densidad es 1,18 g/mL. ¿Cuál es su molaridad?
Datos: A(Cl)=35,5; A(H)=1
Sol: 11,32M ver solución
Problema 12 El Se disuelven 5 g de HCl en 35 g de agua. La densidad de la disolución es 1,06 g/mL. Hallar la concentración de la disolución en : a) % en masa ;b) en g/l ; c) Molaridad Datos: A(Cl)=35,5; A(H)=1
Sol: 12,5% ; 132,49 g/l ; 3,71M ver solución
Problema 13 Determina la masa de hidróxido de sodio (NaOH) comercial, de pureza 90%, necesaria para preparar 100 mL de disolución 1,25 molar. Datos: A(Na)=23; A(O)=16; A(H)=1
Sol: 5,56 g ver solución
Problema 14¿ qué volumen debes de tomar de una disolución 2 M de ácido nítrico HNO3 para preparar 200 cm3 de otra que sea 0,5 M del mismo ácido ?
Datos: A(H)=1;A(N)=14; A(O)=16;
Sol: 0,05 litros ver solución
Fórmula que me simplifica muchos problemas : C1·V1=C2·V2
¿cuándo la puedo usar? ¿Cómo? Ver vídeo explicativo de cómo tengo que usarla y cuando
Vídeo donde explico qué es una DILUCIÓN
Vamos a hacer dos ejemplos con la fórmula que acabamos de ver , el primero usaremos la fórmula y en el segundo no podemos utilizarla , pero como en el vídeo donde la explico entendimos sus claves la modificamos y resolvemos el segundo ejemplo
Ejemplo 1
¿Cómo prepararías 30 mL de una disolución de amoniaco , NH3, 0,2M a partir de una disolución de amoniaco 0,6M ?
Ejemplo 2
Calcula la molaridad de la solución resultante de mezclar 250 ml de solución de HCl 0,20 M con 350 ml de solución de HCl 0,25M Suponiendo que los volúmenes son aditivos
Problema 15 Determina el volumen de ácido clorhídrico comercial, de densidad 1,2 g/mL y pureza el 30%, que hay que tomar para preparar 250 mL de disolución 0,3 M. Datos: A(Cl)=35,5; A(H)=1
Sol: 7,6mL ver solución
Diluciones ejercicios resueltos 1 bachillerato J Ign Con
Determina las molaridades de las disoluciones preparadas mezclando 50 ml de ácido nítrico 0,25 M con:
- a) 80 ml de agua 0,096 M ver solución
- b) 120 ml de ácido nítrico 1,5 M ver solución
continúamos en la siguiente entrada
Fracción molar y molalidad Disoluciones nivel 2 novedad
Presión osmótica Fórmula y ejercicios resueltos
Disoluciones ejercicios de exámenes
otros enlaces que os pueden interesar



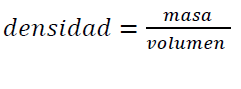
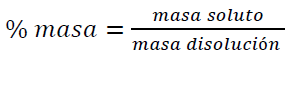
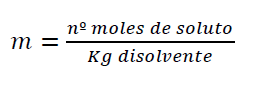







72 comentarios
gracias por la ayuda!!!!!!!!!
Hola tengo dudas para resolver un ejercicio….:Tengo una disolución de 0,280 moles de SO2 paar un volumen de 200 ml., calcula los gramos que son necesarios de SO2, sabiendo que su masa molar es 64.1 gramos/mol.; seguidamente para dicha disolución inicial de SO2, ¿qué deberá hacer si lo que desea es preparar 3,4×10² de una disolución de 2,16 M de SO2?, muchas gracias y un saludo
Enviame el ejercicio a mi correo
Hola Sergio, pues te mandaría el ejercicio…pero no sé el correo…es profesor10demates@gmail.com ???
Muchas gracias
Muchas gracias Sergio por tu ayuda, un saludo.
hola necesito ayuda por favor par resolver esto…
1. El refresco americano llamado “root beer” contiene 0.13 % de una disolución dl 75 % en masa de H3PO4. ¿Cuántos mililitros de fosforo hay en un bote de 12 onzas de este refresco? Suponga una densidad de la disolución de 1.00 g/mL. 1 Onza= 29,6 mL
por favor ayudem se lo agradeceria
Suscribete a mi blog
Cuando lo hagas enviame el ejercicio a mi correo
profesor10demates@gmail.com
El refresco americano llamado “root beer” contiene 0.13 % de una disolución dl 75 % en masa de H3PO4. ¿Cuántos mililitros de fosforo hay en un bote de 12 onzas de este refresco? Suponga una densidad de la disolución de 1.00 g/mL. 1 Onza= 29,6 mL
por favor necesito ayuda con este ejercicio… gracias
suscribete al blog y enviamelo también a mi correo
Muchas gracias me ha ayudado mucho!!!! sigue asi!!
Gracias Silvia
comentarios como el tuyo me animan para seguir trabajando
Como se hace paso a paso .
1.preparar 150ml de disolución saturada de mentol en agua .
Para ello dispongo de 50 g de mentol en polvo ,agua purificada y varios litros de disolución 6N de mentol en agua .
Podré prepararla?
En caso negativo q me falta o me sobra ? En caso positivo que cantidad de disolución 6N de agua purificada usaré ?
Mentol Eq/ g =156
D=0,89g/ml
Coeficiente de solubilidad 490g/L .
Explica porfa .q soy muy tonta .
enviamelo en un correo
Me puedes ayudar cn un problema de disoluciones super facil supongo pero no se hacerlo
Me puedes ayudar con un problema de disoluciones es facil supongo pero no se hacerlo
enviame un correo a profesor10demates@gmail.com
Hola profe qué tal? Pues mira, no consigo solucionar ni plantear bien los problemas de disoluciones cuando entran en los datos, las riquezas y densidades. Sé perfectamente qué significan dichas magnitudes, pero por ejemplo en un problema tan simple como:
Tenemos una disolución de HNO
3
cuya riqueza es del 70% y tiene una densidad de 1.42 g/ml.
Calcular:
a) La molaridad de la disolución. (Resultado: 15.7 M)
b) ¿Qué volumen de esa disolución será necesarios para preparar 300 ml de disolución de
ácido nítrico 2.5 M? (Resultado: 47.5 cm
Pues ahí, ya me pierdo, no sé como atacar el problema.
Te mando el problema por correo?
Un saludo!
enviamelo en un correo
mira primero el ejerccio 11 para el primer apartado
y el 15 para el segundo
1.Una bacteria tiene 0,15% (p / v) de hidrogenofosfato potasico. Indica esta concentración como ppm de hidrogenofosfato potasico.
2.la etiqueta de una botella de leche que contiene 200mg de calcio por cada 100ml de leche. ¿Cuál es la concentración de calcio expresada como% (p / v) de fosfato de calcio?
3.El agua de un circuito de refrigeración tiene una concentración de aluminio de 3N (normalidad). ¿Cuál es la concentración si la expresamos en% de AlPO4?
gracias profepor los problema resueltos
me ayudo mucho sus problemas gracias profesor de peru le estoy muy agradecido
gracias
saludos a Peru
Escelenteeee!!
Hola Sergio,
Estoy contenta de poder contactar contigo, es una gran ayuda …
Excelente !!!!!
Me puedes ayudar?
gracias
Gracias mil gracias. Evacue muchas dudas y pude practicar ejercicios. Me encantó!!! Admiro su trabajo.
muchas gracias
próximamente voy a sacar una serie de ejercicios de disoluciones de exámenes
por favor necesito resolver problemas de densidad volumen y masa me podrian ayudar
POR FAVOR NECESITO AYUDA EN ESTE PROBLEMITA CUANTOSGRAMOS DE SOLUTO HAY DISUELTOS EN 262n DISOLUCION ACUOSA DE HIDROXIDO DE SODIO 0.4 M
Gracias por todo.!!!!!
muy bueno!! sobre todo la foto de perfil!!!,,,ahora enserio la pagina es muy preoductiva,ENHORABUENA SERGIO!!!!
Profe muchas gracias, ojalá que este blog continué y no se desanime, porque mucho de nosotros estariamos perdidos…saludes y agradecimiento desde Colombia
Porfa necesito ayuda del profesor10demates
MUY BUENO!! A mí me ha ayudado mucho con los exámenes. ¡Muchas gracias!
madre mia!!! que descubrimiento!!! me ha ayudado muchísimo esta página para mis exámenes!! explicaciones maravillosas!! muchísimas gracias!!:)
gracias e podido resolver algunas de mis dudas pero no aparece nada acerca de la normalidad … por favor agradecería su ayuda . ..
muchas gracias por las buenas explicaciones que das, tendré que visitar tu pagina más a menudo..
Muchas gracias por esas maravillosas explicaciones, se ve que eres un profesor con vocación,
No cambies nunca. Desde pamplona te envío un cordial saludo.
muchas gracias me lo explicas mejor que mi profesora
Gracias
Hola Profe te envió un problema al correo,ya te sigo ! Necesito tu ayuda
muchisimas gracias
hola
Muchísimas gracias, entendí este tema muy fácil con tus vídeos 😀 , muy agradecido, sigue haciendo vídeos eres grande 😀
Muchísimas gracias. Tengo examen dentro de dos días y no tenía mucha idea, con tus vídeos he terminado de comprender el tema
Muchas gracias. Me sirvió mucho para un parcial de la universidad.
Muchas gracias. Con esto estudié para mi parcial de Química de la universidad. 🙂
muchas gracias
grax man me ha servío de mucho jeej
ggracias
la formula de un compuesto es CH. a 200ºC, si 145 g de este compuesto ocupan 97,2L a una presion de 0,74 atm. ¿Cual es la formula molecular del compuesto? ayudemen es para hoy
Fórmula empírica y molecular
http://profesor10demates.blogspot.com.es/2013/12/formula-empirica-y-molecular.html
ola disculpe pero le envie unos ejercicios a su correo ya me suscribi enserio necesito esos ejercicios urgente
necesitaria que me ayude con unos problemas..cual seria el correo?
Hola Sergio. Me puedes ayudar con esto?
¿Cuántos gramos de ácido sulfúrico tienen 500 mL de una disolución problema?, de la que conocemos que 20 mL de la misma valorándose con fenolftaleína e hidróxido sódico 0,5 N, consumieron exactamente 33.5 mL antes de cambiar el color durante la valoración. Creo que sólo sé hacer una parte de este problema y el 1 tengo examen. Muchas gracias por tu ayuda
lo siento no tengo ninguno parecido
suerte
hola tengo una duda en las formulas para calcular los moles pone gramos/Mm ¿que significa Mm? gracias por la ayuda
Masa molecular
Eres el mejor!!!! Sigue así.
buenos ejercicios
Profesor!! , Me ayudó mucho con sus ejercicios aparte que explica muy bien C: …. Muchas Gracias.
simplemente fantástico 🙂
Manuel…ola me pueden ayudar.el limite de desenso en el agua potable ess de 0.5ppm.! Cuantos equivale este valor en g/ml y molaridad.
Me gustan mucho tus vídeos y bueno yo estoy reciclan-dome sacando el titulo medio de técnico de farmacia y tenemos formulación magistral que no tengo ni idea y necesito aprobarlo… Gracias Sergio, espero que me puedas ayudar.
Hola Sergio me llamo Alberto. Quería decirte que tus vídeos me están ayudando mucho con estos problemas y, por supuesto, agradecértelo, ya que esta parte de la química siempre se me atragantaba.
Profe donde estan los ejercicios de disolucion en soluciones
Hola Sergio, hace una semana estuve toda la tarde haciendo ejercicios de fisica y quimica para el examen que tenia el dia despues. Tus videos me ayudaron mucho y fui la unica de toda la clase que aprobe el examen. Muchisimas gracias.
BUEN TRABAJO
excelentes ejercicios, me han ayudado demasiado, muchas gracias sergio
hola sergio, excelentes tus ejercicios y explicaciones, tambien tienes ejercicios de ph acidos y bases debiles?
willy