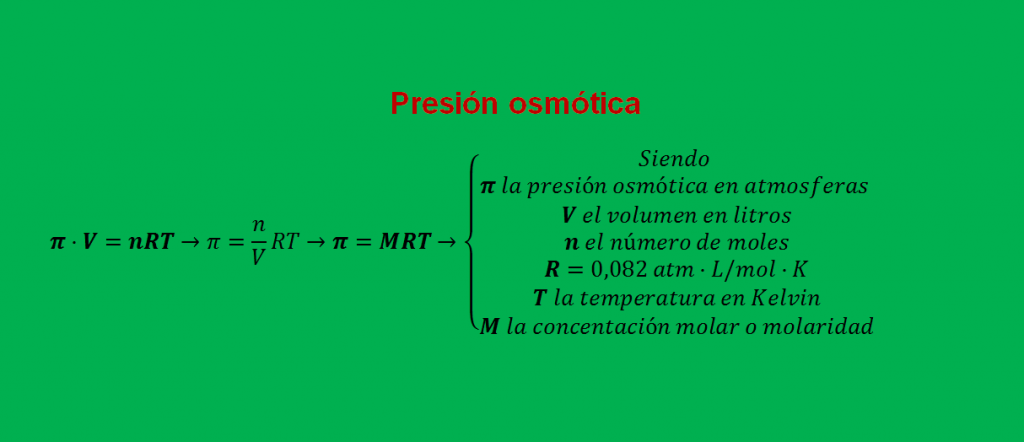
Presión osmótica Fórmula y ejercicios resueltos , propiedades coligativas de las disoluciones. Explicaremos la fórmula de la presión osmótica y realizaremos unos problemas hasta ser unas máquinas . Física y química 1 bachillerato y universidad .
 Recuerda : 1atm=760 mmHg
Recuerda : 1atm=760 mmHg
Ejercicios resueltos 01 ver solución
Calcula la presión osmótica de una disolución que contiene 12 g de sacarosa (C12H22O11) en 500 ml de disolución, a 20 ºC.
Datos : C=12;H=1;O=16
MSI 1 bachillerato
Ejercicios resueltos 02 ver solución
Una disolución de 4,00 g de hemoglobina en 200 ml de disolución tiene una presión osmótica igual a 0,0078 atm, a 20º C. ¿Cuál es la masa molecular de la hemoglobina?
Si ya eres una máquina ayudanos a crecer compartiéndonos por las redes sociales
TEORÍA
En las disoluciones, igual que sucede en los gases, las moléculas de soluto se mueven libremente por el disolvente , ejerciendo una presión sobre las paredes del recipiente que las contiene .
Cuando tenemos dos disoluciones , una concentra y otra diluida , separadas por una membrana semipermeable ( es aquella que solo deja pasar moléculas de disolvente ) se produce el paso de disolvente desde la disolución diluida a la concentrada , a este fenómeno se le llama ósmosis .
La presión osmótica es la presión necesaria para detener la ósmosis.
Esta entrada pertence al curso de Propiedades coligativas desde cero
Para seguir el curso de disoluciones sigue los siguiente enlaces
Fracción molar y molalidad Disoluciones nivel 2
Disoluciones ejercicios de exámenes
Otros enlaces que os pueden interesar
Hidruros No metálicos Hidrácidos curso de formulación inorgánica desde cero
EXAMENES PROBABILIDAD DISTRIBUCION NORMAL Y BINOMIAL
Ejercicios resueltos Derivadas de funciones
Inecuaciones racionales polinomicas Ejercicios de exámenes
Enlace Covalente ejemplos y ejercicios